- 分類:精準醫療
- 作者 陳駿逸
- 點擊數:557
4期胰腺臟癌應儘早進行基因檢測 精準治療療效佳
國家綜合癌症網絡雜誌 (Journal of the National Comprehensive Cancer Network)於2022年報告了1例罕見的攜帶FGFR2基因融合的胰臟導管腺癌患者,精準出擊,使用FGFR標靶藥物erdafintib治療反應佳。基準醫療名白判斷出FGFR基因突變在該名患者所引起的腫瘤生物學變異,以及如何在其致癌過程中的作用,並且協助其探索出更適合的治療。
同時該病例成功之經驗,也告知了年輕的胰臟導管腺癌患者,應該儘早進行基因檢測以確定是否有藥物可靶向的基因突變,如:基因出現融合異常,以期更早啟動恰當的治療,特別是KRAS基因為野生型的,而90%的胰臟導管腺癌都會發生KRAS基因的突變。
研究證實常見的胰臟癌,也就是導管腺癌期在腫瘤微環境中的適應性訊號可以促進腫瘤的增殖和生存,特別是Fibroblast growth factors (FGFs,成纖維細胞生長因子)的訊號傳遞,如此會影響化療藥物的療效,且FGF的訊號傳遞如果過度啟動會協助癌病的惡化。
FGFRs(FGF receptor,成纖維細胞生長因子受體)是具有酪氨酸激酶受體作用的一種跨膜蛋白,參與多種的細胞過程,其遺傳學的改變會產生致癌的信號,直接刺激癌細胞生長,有助於形成新的血管供養腫瘤,促進腫瘤對抗癌藥物的抗藥。
當成纖維細胞生長因子受體的基因出現重排產生了融合基因,特別是成纖維細胞生長因子受體中的FGFR2則會與癌症的發生發展有關,可見於多種癌症類型。
而FGFR2出現基因的融合在肝內膽管癌發生率最高,約為10%-16%,FGFR2突變也可於膽囊癌、乳癌、甲狀腺癌和攝護腺癌出現,只是發生率較低。而大約有5%的胰盎癌具有FGFR成纖維細胞生長因子受體的基因,其中成纖維細胞生長因子受體的基因融合更為罕見。而目前有FGFR的標靶藥物:FGFR1-4小分子抑制劑erdafitinb,目前可以用於化療後進展的FGFR2或FGFR3突變局部晚期或轉移性尿路上皮癌;以及FGFR1-3小分子抑制劑pemigatinib,用於FGFR2融合或重排局部晚期不可切除或轉移性膽管癌。
國家綜合癌症網絡雜誌 (Journal of the National Comprehensive Cancer Network)於2022年的病例報告如下:
28歲男性患者,西班牙裔,因為上腹部疼痛就診,影像學檢查發現胰臟的頭部有一個腫塊,以及多個懷疑為轉移的肝臟和肺部病變。內視鏡超音波顯示胰臟的頭部有一4×3.8cm的低回聲、邊界清楚的腫塊,中心為不規則且為無回聲的囊性成分。粗針穿刺切片證實為低分化的腺癌。
進行超音波導引下的肝臟穿刺切片證實為低分化的腺癌。
患者立即開始使用胰臟癌的化療方案FOLFOXIRI治療,2個月內進行了5個療程的治療。期間醫師建議進行精準醫療,使用胰臟腫瘤組織進行FoundationOne的基因檢測以及Perthera多組學的分析,未發現KRAS突變(也就是屬於KRAS野生型),且檢測到FGFR2基因出現重排,以及CDKN2A和CDKN2B基因有缺失,此外還有多個未明意義的體細胞改變,包括BAP1缺失和FGF14、LTK、MSH2、NOTCH1、PIK3C2B、RICTOR、SOX9和ZNF703突變。
完成FOLFOXIRI治療2個月後,影像複診顯示病情惡化。
此時患者該接受2療程的臨床試驗用藥MGD009-01治療,這是一種雙特異性抗體,作用於B7H3和CD-3表達的腫瘤細胞。然而疾病仍然迅速惡化,尤其是肺部轉移的病變且腹水增多,也出現了新發的左側胸腔積水,肝臟周圍淋巴結病變,多個肺部和肝臟病變略增大。
於是患者開始改用FGFR2抑制劑erdafitinb治療,隨之出現症狀上的改善,體重改善,腹水和高鈣血症緩解,斷層檢查顯示肺部轉移病灶顯著減小, CA 19-9降低。於發表文章時,患者已持續治療有12個月,治療上仍然是反應良好。
該病患對erdafitinb的良好反應,顯示FGFR2基因融合可能是部分胰臟癌患者的治療靶點。既往研究表明,erdafitinib可以有效治療FGFR2或FGFR3 改變的尿路上皮癌和膽管癌,治療有效率分別為40%和50%。但早期體外研究顯示,erdafitinib可以抑制FGFR磷酸化和信號傳導,降低細胞活性,因此靶向FGFR改變(包括融合)成為有效的治療方法。而於2021年也有一份病例報告披露1明68歲的具有FGFR2基因融合之KRAS野生型的胰臟癌,也是在接受erdafitinb的治療,且反應很好。
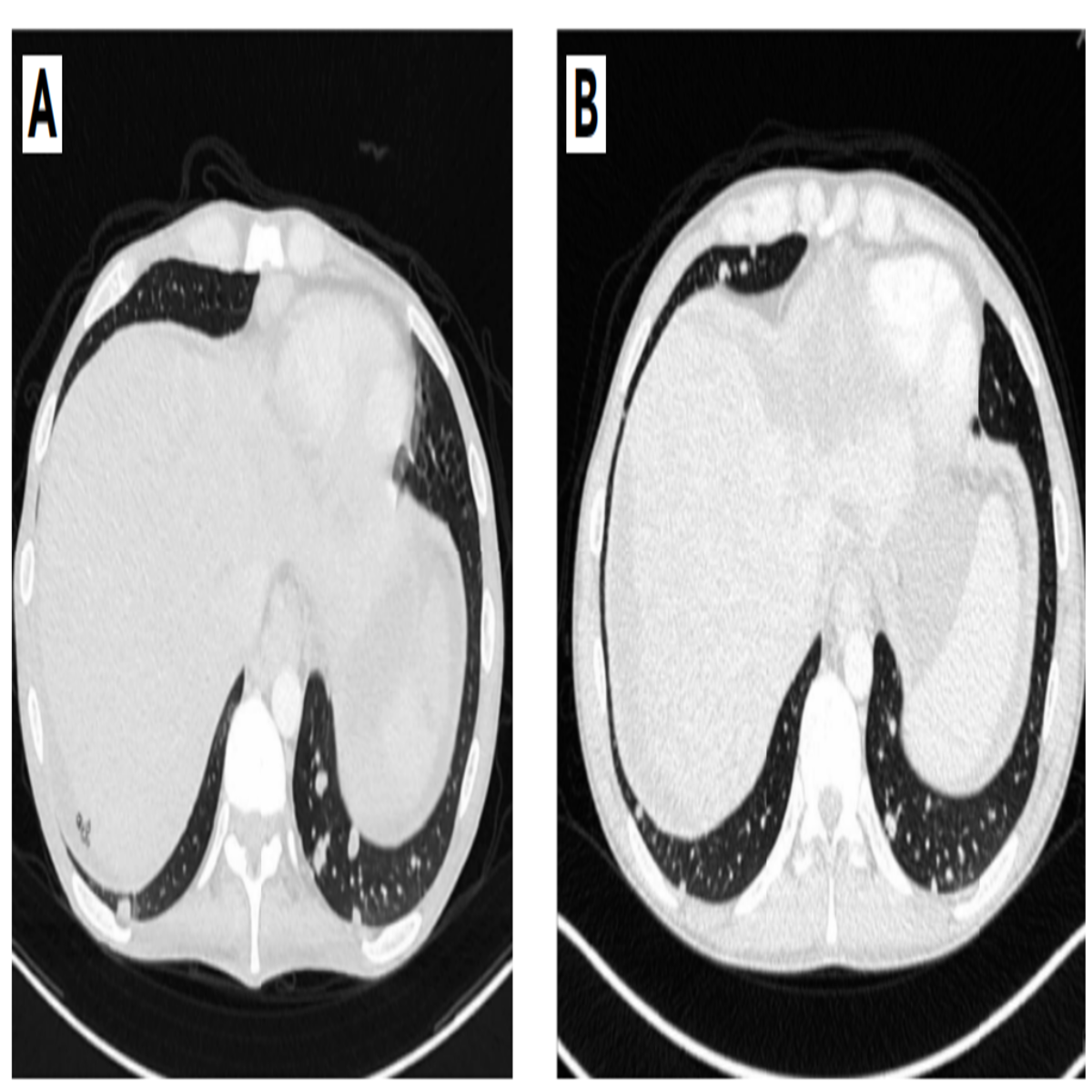
(A)erdafitinb治療前;(B)erdafitinb治療後
FGFR基因的異常在胰臟癌中是很少見的。有一項研究指出,只有4%-6%胰腺癌是FGFR基因異常,尤其是FGFR2基因出現融合更是少見,該報告聲明僅有15例的病例報告。
這名年輕患者為KRAS野生型的胰臟癌,通常胰腺癌中KRAS基因的突變占絕大多數,而KRAS WT野生型的胰臟癌大約只有1成,該案例的意義是告訴我們,對於年輕(<50歲)的KRAS野生型的胰臟癌患者,更可能會有基因融合的異常。有22%的KRAS野生型的胰臟癌被發現具有藥物可靶向的基因變異,如FGFR2、ALK、ROS1、RET和NOTCH1、MET、NRG1和RAF1。另外有一項研究發現,11%KRAS野生型的胰臟癌有基因融合的異常,其中約23%是屬於FGFR2基因融合的異常。
另外有一項研究還報告了5例KRAS野生型的胰臟癌被發現具有ALK融合,年齡32-46歲,該研究認為,這類有ALK基因融合的患者,其特徵是患者年齡較小、且缺少KRAS突變。
而本病例進一步證實,KRAS野生型的胰臟癌的年輕患者,很有可能有其他突變,需要進一步基因檢測方能揭示疾病的可靶向藥物基因突變。鑒於以上資料,建議所有胰臟癌患者都應該儘早進行基因檢測的檢查,確定是否有藥物可以靶向的基因改變,以便採用精準的治療。

#KRAS野生型
#胰臟癌
#基因檢測
#癌症精準醫療
#FGFR
#成纖維細胞生長因子受體
#陳駿逸醫師
#癌歸於好
#知癌抗癌翻轉人生小學堂
#癌症治療
更多陳駿逸醫師的癌症衛教影片請連接 https://mycancerfree.com/videos/
更多腫瘤治療相關資訊 請連接"陳駿逸醫師 與你癌歸於好" https://mycancerfree.com
更多癌症病友需知 請連接"全方位癌症關懷協會" https://www.cancerinfotw.org/index.php
歡迎參與臉書社團:陳駿逸醫師的用心話聊俱樂部 www.facebook.com/groups/456281992960876/
